Il metil salicilato, un composto chimico di notevole importanza, trova le sue radici sia nell'estrazione da fonti naturali sia nella sintesi chimica. La sua storia è intrinsecamente legata a quella dei salicilati in generale, una classe di sostanze che ha rivoluzionato la medicina moderna, in particolare nel campo del trattamento del dolore e dell'infiammazione.
L'Origine Naturale: Gaultheria Procumbens e i Salicilati Vegetali

La Gaultheria procumbens, comunemente nota come Wintergreen o Tè del Canada, è una pianta sempreverde arbustiva appartenente al genere Ericaceae, tipica del Nord America. Questa pianta, alta da 10 cm a 1,5 m, è caratterizzata da frutti e foglie molto resistenti, capaci di superare l'inverno. La Gaultheria procumbens rappresenta una fonte primaria per l'ottenimento del metil salicilato, un olio essenziale profumato che, sebbene apprezzato per le sue proprietà, nasconde un potenziale di grave tossicità per l'uomo.
L'intossicazione da Gaultheria procumbens si verifica tipicamente attraverso l'ingestione accidentale o intenzionale del suo olio essenziale, estremamente concentrato. Una piccola quantità, circa 5 ml, può contenere un quantitativo di salicilato equivalente a quello di oltre 20 compresse di aspirina per adulti, rendendolo uno dei veleni vegetali più insidiosi. Il meccanismo d'azione della Gaultheria procumbens si basa sul salicilato di metile, che viene rapidamente assorbito attraverso le mucose gastriche e persino attraverso la pelle, convertendosi in acido salicilico nel sangue. La causa primaria di intossicazione è l'esposizione impropria all'olio essenziale, il cui odore gradevole e dolciastro, simile a quello di caramelle o gomme da masticare, lo rende particolarmente pericoloso per i bambini piccoli.
La diagnosi di intossicazione da Gaultheria procumbens si fonda su un'attenta anamnesi, che indaga la storia di esposizione alla pianta o all'olio, e sulla valutazione clinica dei sintomi. L'esame fondamentale è la misurazione dei livelli sierici di salicilato. In caso di ingestione recente (entro 1-2 ore), può essere somministrato carbone attivo per limitare l'assorbimento del salicilato nel tratto gastrointestinale. L'alcalinizzazione urinaria, mediante somministrazione endovenosa di bicarbonato di sodio, è cruciale. Nei casi di intossicazione severa, caratterizzata da livelli molto alti di salicilato, insufficienza renale, alterazioni persistenti dello stato mentale o edema polmonare, l'emodialisi rappresenta il trattamento d'elezione. Se non trattata, l'intossicazione può condurre a edema cerebrale, collasso cardiovascolare e morte. In caso di esposizione cutanea massiccia seguita da malessere, è altrettanto urgente una valutazione medica professionale.
Oltre alla Gaultheria procumbens, i salicilati sono presenti in altre specie vegetali, in particolare nella corteccia di alcuni salici (come Salix alba, Salix fragilis) e in altre piante del genere Spiraea, ma anche in Cassia aeutifolia, Polygala senega e Dorema ammoniacum. In queste piante, i salicilati si trovano sotto forma di glicosidi, principalmente la salicina, un glucoside formato da glucosio e alcool salicilico.
Dalla Salicina all'Acido Salicilico: Una Scoperta Storica
La storia dell'isolamento dei salicilati è un percorso affascinante che attraversa diversi secoli e coinvolge numerosi scienziati. I primi tentativi di isolare il principio attivo dalla corteccia del salice risalgono a William White, farmacista di Bath. Ulteriori resoconti medici sugli effetti antipiretici e analgesici del salice si hanno nel 1772 (Gunzius), nel 1778 (van Geuns), nel 1792 (Samuel James) e nel 1803 (Wilkinson).
Il primo isolamento della salicina è tradizionalmente attribuito al farmacista tedesco Johann Andreas Buchner nel 1828. Tuttavia, secondo la storia dell'aspirina edita da Schindler nel 1979, gli italiani Fontana e Brugnatelli avevano raggiunto lo stesso risultato due anni prima, nel 1826. Dopo Buchner, il francese Leroux isolò anch'egli la salicina e ne dimostrò l'attività antipiretica. Successivamente, nel 1933, anche Merck riportò l'isolamento della salicina a partire dalla corteccia di salice.
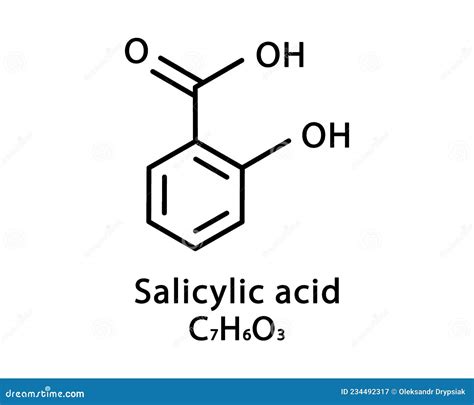
Il primo ad ottenere l'acido salicilico fu, nel 1835, il chimico svizzero Carl Jacob Löwig, che lo isolò e purificò a partire dalla Spiraea ulmaria (la regina dei prati). Lo stesso risultato fu ottenuto a Parigi nel 1838 da Piria, partendo dalla corteccia di salice. Un anno dopo, Dumas dimostrò come i composti di Löwig e Piria fossero identici. L'acido salicilico, un composto che presenta due importanti gruppi funzionali: un fenolo e un acido carbossilico, divenne il fulcro di ulteriori ricerche.
Aspirina : la pillola che ha cambiato il mondo
La Nascita dell'Aspirina: Un'Innovazione Farmaceutica
Dall'isolamento dei salicilati da fonti naturali, il loro uso iniziò a diffondersi e divenne ben noto ed accettato. Ulteriori conferme degli effetti dell'acido salicilico e del salicilato di sodio si ebbero in Francia e negli Stati Uniti. Tuttavia, l'acido salicilico presentava un effetto collaterale significativo: irritazione della mucosa gastrointestinale.
Nel 1897, il chimico Felix Hoffman, ricercatore presso la Bayer, iniziò a lavorare alla ricerca di un sostituto meno irritante. È generalmente accettato che egli si occupò di questo argomento in quanto suo padre aveva accusato gli effetti collaterali del salicilato di sodio, che assumeva per curare i reumatismi. Il 10 ottobre del 1897, egli sintetizzò l'acido acetilsalicilico (acetilando l'ossidrile fenolico) facendo reagire l'acido salicilico a riflusso con l'anidride acetica. Il composto fu inviato ai test farmacologici, dove ottenne risultati molto positivi, e successivamente ai test clinici. L'acido acetilsalicilico (AAS), commercializzato con il nome di Aspirina, derivato dal nome tedesco del composto (Acetylspirsäure), segnò una svolta nella terapia del dolore e dell'infiammazione.
Meccanismi d'Azione e Usi Terapeutici dei Salicilati
Sebbene i salicilati fossero impiegati in clinica da quasi un secolo, solo nel 1971 fu chiarito il loro meccanismo d'azione. Sono state individuate tre diverse isoforme della Prostaglandina-endoperossido sintasi o cicloossigenasi (COX), l'enzima responsabile della sintesi di prostaglandine, prostacicline e trombossani. La scoperta della COX-2, in particolare, ha aperto nuove prospettive terapeutiche, poiché tale isoforma è inducibile e responsabile della risposta infiammatoria, mentre la COX-1, costitutiva, secerne prostacicline con funzioni di mantenimento a livello gastrico.
I principali effetti dei salicilati sono l'analgesia, l'attività antipiretica e antinfiammatoria. I salicilati sono usati per la loro attività analgesica più di ogni altra classe di farmaci, in particolare come analgesici periferici. L'attività più nota dei salicilati è quella antinfiammatoria.
L'inibizione delle ciclossigenasi è il meccanismo d'azione comunemente accettato per l'attività dei salicilati, che sono responsabili della biosintesi di prostaglandine. L'acido acetilsalicilico, in particolare, inibisce le ciclossigenasi mediante un legame covalente, mentre altri salicilati instaurano interazioni deboli.
Molti sforzi sono stati compiuti nel tentativo di limitare gli effetti collaterali dei salicilati sul sistema gastrointestinale, mantenendone l'attività antinfiammatoria, analgesica e antipiretica. Tuttavia, l'acido acetilsalicilico sintetizzato da Hoffman nel 1897 rimane il composto con il miglior profilo farmacologico. L'attività sembra essere legata all'anione salicilato, mentre la tossicità gastrica è data dalla funzionalità acida; non è pertanto possibile ottenere attività senza effetti collaterali.
L'Uso dei Salicilati nella Popolazione Pediatrica e le Precauzioni
Il rapporto rischio/beneficio e la disponibilità di valide alternative terapeutiche fanno sì che, nella popolazione pediatrica, i salicilati siano controindicati. Rimangono farmaci d'elezione (l'acido acetilsalicilico in particolare) solo nel trattamento delle febbri reumatiche e della sindrome di Kawasaki.
L'uso dei salicilati è stato introdotto prima che fosse noto il loro meccanismo d'azione, il che ha favorito, nel tempo, la formazione di diverse teorie per spiegarne i molteplici effetti. L'introduzione di alogeni nell'anello salicilico aumenta sia l'attività sia la tossicità, mentre lo spostamento dell'idrossile in meta o para porta alla perdita dell'attività. L'introduzione di residui aromatici in posizione 5, come nel diflunisal, incrementa l'attività anti-infiammatoria, mentre la riduzione dell'acidità, ad esempio attraverso l'esterificazione, può influenzare il profilo farmacologico.
Assorbimento, Distribuzione, Metabolismo ed Escrezione dei Salicilati
In seguito a somministrazione orale, i salicilati sono assorbiti rapidamente, principalmente a livello gastrico e nella prima parte dell'intestino tenue. Il sito di assorbimento dipende dalla forma farmaceutica: le compresse gastroresistenti portano a un assorbimento esclusivamente intestinale. Il pH gioca un ruolo chiave nell'assorbimento di farmaci ionizzabili come i salicilati, in quanto la forma assorbita è quella protonata (neutra), più lipofila e capace di attraversare le membrane cellulari.
I salicilati si legano significativamente (80-90%) alle proteine plasmatiche, in particolare all'albumina serica. In caso di ipoalbuminemia, condizione riscontrabile nell'artrite reumatoide, la concentrazione di farmaco libero può risultare maggiore.
Tutti i derivati esterei e la salicilammide sono più o meno rapidamente idrolizzati ad acido salicilico, mentre i sali sono già in equilibrio acido/base con la forma protonata. Solo il 10% dell'acido salicilico viene escreto come tale nelle urine; il restante 90% è metabolizzato principalmente attraverso coniugazione con acido glucuronico e glicina (metabolismo di fase II). Le reazioni di fase I (ossidazione microsomiale epatica) sono minoritarie, rappresentando solo circa il 5% del metabolismo totale.
Tossicità e Interazioni Farmacologiche dei Salicilati
Livelli ematici di salicilati superiori a quelli terapeutici possono causare tossicità acuta e cronica. Agendo direttamente sul centro del respiro a livello del midollo allungato, i salicilati provocano un aumento della frequenza respiratoria che porta all'alcalosi respiratoria. Ne consegue un'aumentata escrezione renale di anioni carbonato, seguita da cationi sodio e potassio. La perdita di sali favorisce la disidratazione per osmosi e una ridotta capacità tampone ematica. La natura acida dei salicilati e dei loro metaboliti causa acidosi sistemica, che influenza il metabolismo cellulare.
In caso di assunzione di dosi eccessive di salicilati, se l'evento è avvenuto nell'ora precedente, il trattamento d'elezione è la lavanda gastrica.
La sindrome di Reye è una condizione acuta rara (0,15 casi ogni 100.000 ragazzi sotto i 18 anni), fatale nel 20-30% dei casi, secondaria all'assunzione di salicilati in soggetti di età pediatrica. Si verifica in particolare nei bambini sotto i 12 anni affetti da varicella o sindromi simil-influenzali trattati con salicilati.
Tra gli effetti collaterali più comunemente riportati dei salicilati vi sono disturbi del tratto gastrointestinale: nausea, vomito, disturbi epigastrici, bruciore di stomaco, ulcerazioni, gastriti ed emorragie gastrointestinali. Le emorragie gastrointestinali possono essere indolori e sono possibili anche a bassi dosaggi, e secondo alcuni studi non dipendono tanto dal dosaggio quanto dalla frequenza di assunzione del farmaco. L'incidenza di questi disturbi può essere drasticamente ridotta con la co-somministrazione di un inibitore della pompa protonica.
L'ampio uso dei salicilati, e dell'aspirina in particolare, ha portato all'individuazione di numerose interazioni con altri farmaci, talvolta clinicamente significative. Le interazioni farmacologiche a livello della distribuzione riguardano principalmente il legame alle proteine plasmatiche. Le caratteristiche di acidi deboli dei salicilati fanno sì che, al pH ematico, essi siano prevalentemente deprotonati e pertanto si leghino all'albumina serica. Ciò può comportare competizione e spiazzamento con altri farmaci fortemente legati all'albumina, come gli anticoagulanti orali (warfarin), sommando all'azione anticoagulante propria dei salicilati.
Per quanto riguarda il metotrexato, l'interazione con i salicilati è nota da tempo. Inizialmente si riteneva che il meccanismo principale fosse la competizione per il legame alle proteine sieriche. Successivamente è stato dimostrato come sia più importante l'interazione a livello dell'escrezione: l'inibizione della sintesi di prostaglandine da parte dei salicilati riduce il flusso ematico renale, e quindi la filtrazione glomerulare di metotrexato. Inoltre, i salicilati inibiscono la secrezione tubulare di metotrexato. A cavallo del nuovo millennio, studi in vitro hanno evidenziato l'esistenza di molti trasportatori a livello renale per i FANS e per il metotrexato.
I corticosteroidi, invece, a causa dell'aumentata filtrazione glomerulare, aumentano l'escrezione di salicilati.
La Regina dei Prati (Spiraea ulmaria) e il suo Ruolo

La regina dei prati (Spiraea ulmaria), nota anche come olmaria, è una pianta erbacea perenne e mellifera degli ambienti umidi, comune in Europa, Asia e America. Il nome latino "Spiraea" deriva dalla forma a spirale dei suoi frutti. La scoperta dell'acido salicilico a partire da questa pianta ha dato il nome all'aspirina (A per "acetile" e spir per "spirea").
Le sommità fiorite sono le parti utilizzate in terapia, raccolte in giugno/luglio all'inizio della fioritura. La regina dei prati contiene acido ascorbico, cumarina, flavonoidi (spiraeoside, rutina, iperoside e avicularina), eparina, mucillagini, acidi fenolici e glicosidi fenolici (inclusi la spiraeina, la monotropina e la gaulterina).
Grazie alle sue proprietà diuretiche e antinfiammatorie, la regina dei prati è raccomandata nella prevenzione della gotta. Essa permette di trattare i sintomi del raffreddore, come febbre e mal di testa, grazie al suo alto contenuto di acido salicilico. L'EMA (Agenzia Europea per i Medicinali) e l'ESCOP (European Scientific Cooperative on Phytotherapy) la raccomandano come rimedio tradizionale a base di piante per il trattamento di supporto del raffreddore e per il sollievo dei dolori articolari lievi. La spirea è tradizionalmente utilizzata anche per trattare i disturbi gastro-intestinali associati all'iperacidità, come la gastrite, la dispepsia acida e l'ulcerazione gastroduodenale.
L'aldeide salicilica, un precursore per la produzione di acido acetilsalicilico, è stata isolata in grande quantità dai boccioli fiorali della regina dei prati. Le salicine nella spirea, trasformate in acido salicilico dopo l'assorbimento, riducono la sintesi delle prostaglandine e dei trombossani inattivando la ciclo-ossigenasi. Inoltre, grazie al suo elevato contenuto di tannini, la spirea esercita in vitro una forte attività inibitoria dell'elastasi, enzima che può avere un ruolo patologico in diverse condizioni.
I fiori della spirea contengono eparina legata a proteine vegetali, conferendo al complesso una significativa attività anticoagulante e fibrinolitica. Gli estratti di spirea possiedono elevate attività antiossidanti, utili anche come conservante. I flavonoidi e l'acido salicilico presenti nella pianta hanno effetti antibatterici, in particolare contro stafilococchi ed Escherichia coli. La spirea è anche astringente, provocando una diminuzione della permeabilità capillare, vasocostrizione locale e azione antidiarroica.
Estratti di radici, erbe e fiori della spirea sono stati studiati per i loro effetti immunomodulatori, in particolare sul sistema del complemento e sulla proliferazione delle cellule T. La decozione della spirea si è dimostrata efficace nella prevenzione delle lesioni gastriche indotte dall'acido acetilsalicilico nei ratti e ha favorito la guarigione delle ulcere gastriche croniche.
Interazioni e Controindicazioni della Regina dei Prati
È necessario prestare attenzione alle interazioni tra la regina dei prati e alcuni farmaci. Alcuni antibiotici come la tetraciclina o la penicillina possono interagire con la regina dei prati, aumentando il rischio di sanguinamenti. Anche il paracetamolo può avere un'interazione debole che aumenta il rischio di sanguinamenti. In teoria, la regina dei prati potrebbe avere un effetto additivo con altri farmaci contenenti salicilati come l'aspirina, sebbene la salicina non sembri avere gli stessi effetti antipiastrinici dell'aspirina. È necessario adattare il dosaggio dei farmaci antinfiammatori non steroidei (FANS) e degli anticoagulanti in caso di associazione con la regina dei prati.
La spirea è da evitare in donne che allattano, in quanto può aumentare il tono uterino e stimolare l'attività uterina. È inoltre controindicata in soggetti allergici ai derivati salicilici (aspirina) o in coloro che devono evitare l'aspirina per altre ragioni. Vi è la possibilità di nefrotossicità quando la spirea è associata al paracetamolo. In teoria, la spirea potrebbe esacerbare l'asma a causa dei suoi effetti broncospastici.
Il Metil Salicilato come Messaggero Chimico Vegetale
In periodi di siccità o temperature "fuori stagione", le piante stressate rilasciano metil salicilato. Questa scoperta è la prova tangibile di una comunicazione pianta-pianta a livello di ecosistema. Le piante, attraverso modifiche al loro metabolismo secondario, sono in grado di adeguarsi all'ambiente circostante. Ogni cambiamento rilevante innesca modifiche nella produzione di metaboliti secondari, spiegando perché gli oli essenziali non siano sempre identici.
La produzione di salicilato di metile ha una duplice funzione per le piante: da un lato, attiva una risposta immunitaria nota come "resistenza sistemica acquisita", aiutando la pianta a reagire meglio allo stimolo stressante e a guarire più rapidamente. Dall'altro, funge da strumento di comunicazione tra le piante, avvisandole reciprocamente del pericolo. Questo fenomeno sottolinea la complessità e la dinamicità della vita vegetale e la variabilità intrinseca degli oli essenziali, che riflettono le condizioni ambientali e le "annate" di produzione.
L'Acido Salicilico: Un Composto Versatile
L'acido salicilico è il più importante dei tre acidi ossibenzoici (orto-meta-para), sia dal punto di vista scientifico sia per le sue applicazioni terapeutiche e industriali (materie coloranti, profumi, conservazione di cibi e bevande, conceria). Ottenuto per la prima volta da R. Piria nel 1838 dalla salicina, esiste in molte piante, più diffusamente come estere metilico (Gaultheria procumbens, tuberosa, acacie, poligale, spiree) o come glucoside (gaulterie, betulla).
Un tempo si otteneva dalla saponificazione dell'olio di gaulteria. Oggi si prepara industrialmente seguendo processi sintetici modificati. L'acido salicilico cristallizza in aghi bianchi, di sapore acido dolciastro, poco solubile in acqua fredda, più nella calda, molto in alcool ed etere. È volatile al vapor d'acqua.
L'acido salicilico può dare con i metalli alcalini sali neutri e acidi. Alcuni metalli bivalenti e il bismuto danno anche sali basici, mentre il ferro forma vari composti complessi. Per eterificazione dell'ossidrile fenico dell'acido salicilico si ottengono eteri. In relazione alla doppia funzione di fenolo e di acido, si possono avere tre tipi principali di esteri.
Per la ricerca analitica dell'acido salicilico si utilizzano varie reazioni cromatiche, come quella con cloruro ferrico (colorazione violetta), solfato di rame (colorazione verde smeraldo) e il reattivo di Millon (colorazione rossa intensa).
In medicina, l'acido salicilico e i suoi sali sono utilizzati, ma sono stati preparati sinteticamente derivati di notevole importanza terapeutica. L'acido salicilico è un rimedio efficace e quasi specifico del reumatismo articolare acuto, è un buon antipiretico e un pregevole antisettico. Tuttavia, in dosi superiori alla terapeutica o per un uso prolungato, può alterare la digestione, ledere l'epitelio renale, influenzare i normali processi del ricambio e provocare disturbi visivi, uditivi o altri fenomeni nervosi. Per questo motivo, in molti paesi è vietato il suo uso per la conservazione di marmellate e altre derrate alimentari.
L'acido salicilico, che non è assorbito attraverso la pelle intatta, esercita una notevole attività cheratolitica sullo strato corneo dell'epidermide, venendo perciò usato per distruggere le neoformazioni callose. Nell'uomo si elimina in parte come tale, in parte sintetizzato con la glicocolla (acido salicilurico); nel cane si trasforma in parte in acido ossisalicilico.
Fitoterapia e Dolori Reumatici
Per quanto sia fondamentale ribadire che la terapia dei dolori reumatici è di esclusiva competenza medica, può essere utile valutare la "proposta" della fitoterapia. Le piante utili nel trattamento dei dolori reumatici devono possedere la capacità di intervenire sull'infiammazione e sul dolore.
Tra le piante a salicilati o "glicosidi salicilici" si distinguono il salice (Salix alba), l'olmaria (Spiraea ulmaria), la Gaultheria procumbens e la Boswellia. I glicosidi salicilici presenti in queste piante forniscono in vivo derivati con nota attività antinfiammatoria e antireumatica come il salicilato di metile o l'acido salicilico. Il loro meccanismo d'azione prevede il blocco del processo della cicloossigenasi.
Altre piante interessanti includono l'Harpagophytum procumbens (artiglio del diavolo), i cui principi attivi (arpagide, arpagoside, procumbide) hanno proprietà antireumatiche e antiflogistiche simili ai FANS, ma prive degli effetti collaterali. Il meccanismo d'azione sembra legato all'azione diretta della pianta a livello delle terminazioni nervose periarticolari e sulla riduzione della liberazione di sostanze pirogene come chinine e prostaglandine. L'Harpagophytum può essere assunto anche per lunghi periodi senza effetti indesiderati, ma è sconsigliato in gravidanza e in soggetti con ulcera gastrica o duodenale.
La Boswellia serrata, grazie ai suoi acidi boswellici, inibisce l'attività della 5-lipoossigenasi, enzima responsabile della sintesi dei leucotrieni, importanti mediatori dei processi infiammatori articolari.
Piante come il tarassaco (Taraxacum officinale) e l'ortica (Urtica dioica) sono utili per stimolare il tessuto interstiziale, il fegato e i reni, favorendo la diuresi e la coleresi. Cure stagionali a base di tarassaco riducono la rigidità articolare. L'ortica, considerata un diuretico, è un valido rimedio contro il reumatismo e la gotta, favorendo l'eliminazione degli acidi urici.
In conclusione, il metil salicilato e i salicilati in generale rappresentano un capitolo fondamentale nella storia della medicina e della chimica, con un'eredità che continua a influenzare la ricerca e la terapia del dolore e dell'infiammazione, sia attraverso la sintesi chimica che l'utilizzo di fonti naturali.
tags: #6 #metil #salicilato #pianta