La sintesi dell'acido acetilsalicilico, comunemente noto come aspirina, rappresenta un esperimento chimico didattico e accessibile, particolarmente gratificante quando si presta attenzione alla fase cruciale di purificazione tramite cristallizzazione. Questo articolo esplora in dettaglio il processo, le considerazioni pratiche e le proprietà dell'acido salicilico e del suo derivato acetilato, basandosi su procedure consolidate e sull'esperienza diretta.
Il Processo di Sintesi: Un Approccio Metodico
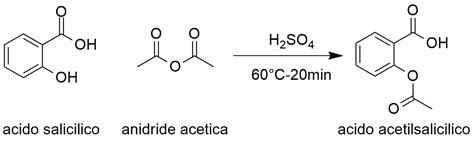
La sintesi dell'acido acetilsalicilico è un processo relativamente semplice che richiede reagenti comuni e attrezzatura di laboratorio standard. Una procedura efficace, basata su quella proposta da Garlaschelli, prevede i seguenti passaggi e materiali:
Materiali Occorrenti:
- Acido salicilico
- Anidride acetica
- Acido solforico concentrato
- Etanolo
- Semplice vetreria di laboratorio (beuta, becker, imbuto Büchner, pompa da vuoto)
Procedura Dettagliata:
- Reazione Iniziale: In una beuta da 250 ml, si pongono 7 grammi di acido salicilico. A questo si aggiungono 10 ml di anidride acetica e, successivamente, 7 gocce di acido solforico concentrato. È fondamentale mescolare bene la miscela per garantire un'omogenea distribuzione dei reagenti.
- Riscaldamento a Bagno Maria: La beuta viene quindi posta con il fondo immerso in un becker da 600 ml contenente una piccola quantità di acqua. Il sistema viene scaldato a bagno maria a una temperatura di circa 60 °C, agitando la miscela di tanto in tanto. Il riscaldamento prosegue per circa dieci minuti.
- Formazione del Prodotto Grezzo: Al termine del riscaldamento, la miscela viene lasciata raffreddare. Durante questo processo, il liquido tende a solidificare, trasformandosi in una massa solida di colore bianco.
- Prima Purificazione (Lavaggio): Al solido formatosi, si aggiungono 100 ml di acqua fredda. La massa solida viene quindi filtrata utilizzando una pompa da vuoto e un imbuto Büchner. Il solido viene spremuto accuratamente per rimuovere quanta più acqua possibile. Successivamente, il solido viene lavato tre volte, utilizzando 15 ml di acqua fredda per ciascun lavaggio, aspirando bene dopo ogni aggiunta per massimizzare la rimozione delle impurità solubili.
- Cristallizzazione: Il solido così ottenuto viene sciolto in 18 ml di etanolo a caldo. È importante assicurarsi che tutto il solido si dissolva completamente. La soluzione calda viene quindi versata in 40 ml di acqua calda. Se necessario, si può riscaldare leggermente la soluzione fino a completa dissoluzione.
- Formazione dei Cristalli: La soluzione viene lasciata raffreddare lentamente. Durante questo raffreddamento, si osserva la separazione di cristalli prismatici di notevole bellezza.
- Filtrazione e Asciugatura Finale: I cristalli formati vengono filtrati nuovamente su Büchner, lavati con piccole porzioni di acqua fredda per rimuovere eventuali tracce di etanolo o impurità residue, e infine lasciati asciugare all'aria.
Un prodotto finale di successo dovrebbe presentarsi perfettamente inodore, di un bianco candido e ben cristallizzato. Il punto di fusione atteso per l'acido acetilsalicilico puro è di circa 136 °C.
Considerazioni Pratiche e Sfide nella Sintesi
La sintesi dell'acido acetilsalicilico, sebbene concettualmente semplice, può presentare delle sfide pratiche che richiedono attenzione. Una delle criticità più frequentemente riscontrate riguarda la qualità dell'anidride acetica utilizzata.
La Criticità dell'Anidride Acetica
L'anidride acetica è un reagente essenziale per la reazione di acetilazione dell'acido salicilico. La sua efficacia dipende dalla sua purezza e dalla sua stabilità. È stato osservato che vecchi lotti di anidride acetica possono degradarsi, principalmente per idrolisi, trasformandosi in acido acetico. Questo processo riduce significativamente la capacità dell'anidride acetica di reagire efficacemente, portando a rese basse o addirittura al fallimento della sintesi.
Segnali di Anidride Acetica Degradata:
- Mancanza di Reazione: Se la reazione non procede come previsto, con scarsa o nulla formazione di prodotto, è probabile che l'anidride acetica sia il colpevole.
- Analisi dei Reagenti: In casi dubbi, un'analisi più approfondita dei reagenti può confermare la presenza di acido acetico al posto dell'anidride acetica.
La gestione dell'anidride acetica nei laboratori richiede particolare attenzione. In molti contesti, l'acquisto e la detenzione di anidride acetica sono soggetti a controlli normativi, data la sua potenziale applicazione nella sintesi illecita di sostanze stupefacenti. Questo implica che i laboratori autorizzati devono documentare rigorosamente l'uso di questo reagente. La disponibilità di anidride acetica di buona qualità è quindi un prerequisito fondamentale per la riuscita di questa sintesi.
FILTRAZIONE metodi separazione laboratorio chimica
L'Acido Salicilico: Proprietà e Applicazioni
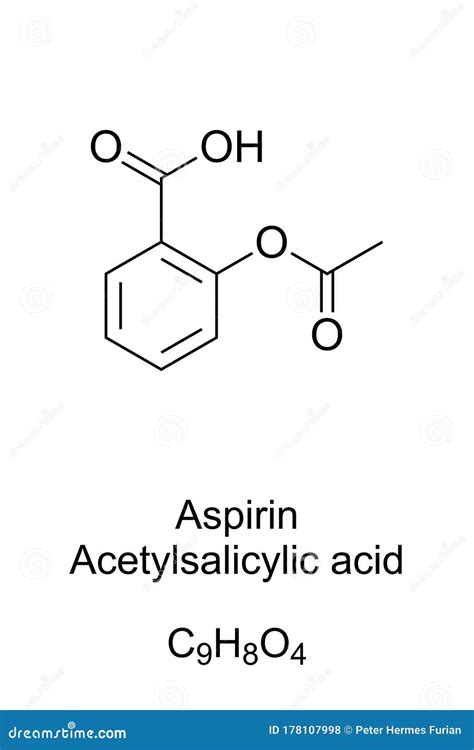
Prima di addentrarci nella sua acetilazione, è utile comprendere le caratteristiche dell'acido salicilico stesso. L'acido salicilico (acido 2-idrossibenzoico) è un composto organico cristallino, incolore, appartenente alla classe degli acidi carbossilici. La sua formula chimica è HOC₆H₄COOH.
Origini e Scoperta
Le proprietà terapeutiche dell'acido salicilico erano note fin dall'antichità. Tradizionalmente, veniva estratto dalla corteccia di alberi del genere Salix (da cui deriva il suo nome), in particolare dal salice bianco (Salix alba). La salicina, un glicoside presente in questi alberi, è stata successivamente identificata come precursore dell'acido salicilico.
Proprietà Chimiche e Reattività
Il gruppo carbossilico (-COOH) presente nella molecola dell'acido salicilico è responsabile della sua acidità e della sua capacità di reagire con gli alcoli per formare esteri. La reazione con il metanolo, ad esempio, porta alla formazione del salicilato di metile, un composto noto per il suo odore caratteristico e presente in oli essenziali come quello della Gaultheria procumbens.
Applicazioni Terapeutiche e Dermatologiche
Sebbene l'acido salicilico puro possa essere tossico se ingerito in grandi quantità, trova ampio impiego in diverse applicazioni quando utilizzato in concentrazioni appropriate:
- Conservante Alimentare: Le sue proprietà antisettiche lo rendono utile nella conservazione di alcuni alimenti.
- Prodotti per l'Igiene Orale: Viene impiegato come antisettico in alcuni dentifrici.
- Dermatologia: L'acido salicilico è un ingrediente chiave in molti prodotti per la cura della pelle, grazie alle sue proprietà cheratolitiche (capacità di sciogliere la cheratina). È efficace nel trattamento di condizioni come l'acne, la cheratosi attinica, le verruche e la psoriasi. Soluzioni alcoliche al 6% sono comunemente utilizzate per questi scopi.
- Farmaci Anti-infiammatori: Estratti contenenti salicina sono stati storicamente utilizzati come agenti antinfiammatori, specialmente nel trattamento dell'artrite reumatoide.
Ruolo nelle Piante
L'acido salicilico svolge anche un ruolo importante come ormone vegetale. Nelle cellule vegetali, viene sintetizzato a partire dalla fenilalanina e partecipa a diversi processi fisiologici, tra cui la risposta immunitaria delle piante (SAR - Systemic Acquired Resistance) contro agenti patogeni. Stimola la respirazione cianuro-resistente e è implicato nell'attivazione di geni che codificano per proteine di difesa.
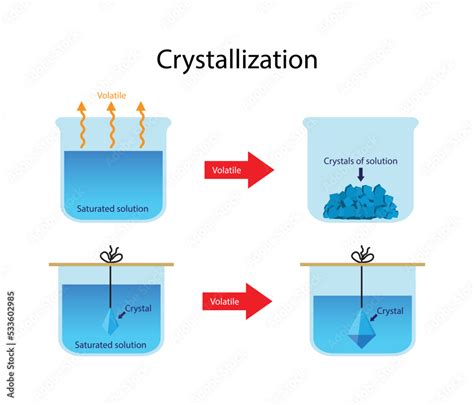
La Cristallizzazione come Metodo di Purificazione
La cristallizzazione è una tecnica fondamentale nella chimica organica per purificare composti solidi. Il principio alla base di questo metodo è la differenza di solubilità tra il composto desiderato e le sue impurità in un dato solvente o miscela di solventi a diverse temperature.
Principi della Cristallizzazione
- Dissoluzione: Il composto grezzo viene disciolto in una quantità minima di solvente caldo, sufficiente a ottenere una soluzione satura o quasi satura. Idealmente, il composto desiderato dovrebbe essere molto solubile nel solvente caldo e poco solubile nel solvente freddo, mentre le impurità dovrebbero avere una solubilità opposta o molto elevata in entrambe le condizioni.
- Raffreddamento Lento: La soluzione calda viene lasciata raffreddare lentamente. Man mano che la temperatura diminuisce, la solubilità del composto desiderato si riduce, portando alla sua precipitazione sotto forma di cristalli puri. Un raffreddamento lento favorisce la formazione di cristalli più grandi e meglio formati, escludendo più efficacemente le impurità.
- Filtrazione: I cristalli formati vengono separati dal liquido madre (la soluzione rimanente, che contiene le impurità più solubili) mediante filtrazione.
- Lavaggio: I cristalli vengono lavati con una piccola quantità di solvente freddo per rimuovere eventuali tracce di liquido madre aderenti alla loro superficie.
- Asciugatura: Infine, i cristalli vengono asciugati per rimuovere il solvente residuo.
Nel caso della sintesi dell'acido acetilsalicilico, la sequenza di dissoluzione in etanolo caldo e successiva aggiunta di acqua calda crea una miscela solvente in cui l'acido acetilsalicilico è meno solubile rispetto alla miscela etanolo-acqua a temperatura ambiente, favorendo così la sua cristallizzazione.
Il Prodotto Finale: Caratteristiche e Verifica
Un acido acetilsalicilico sintetizzato e purificato con successo dovrebbe possedere caratteristiche ben definite:
- Aspetto: Cristalli bianchi, prismatici.
- Odore: Perfettamente inodore. La presenza di odori pungenti potrebbe indicare la presenza di acido acetico residuo o di anidride acetica non reagita.
- Punto di Fusione: Circa 136 °C. Un punto di fusione più basso o un intervallo di fusione ampio sono indicatori di impurità.
La verifica del punto di fusione è un metodo rapido ed efficace per valutare la purezza del prodotto ottenuto.
Considerazioni sulla Sicurezza e sulla Normativa
È importante sottolineare che la manipolazione di reagenti chimici come l'acido solforico concentrato e l'anidride acetica richiede precauzioni di sicurezza adeguate. L'uso di occhiali protettivi, guanti e camice da laboratorio è indispensabile. Inoltre, come accennato in precedenza, l'anidride acetica è una sostanza soggetta a controlli normativi in molte giurisdizioni, e il suo utilizzo deve essere conforme alle leggi vigenti.
L'Acido Acetilsalicilico come Farmaco
L'acido acetilsalicilico è uno dei farmaci più conosciuti e utilizzati al mondo. La sua efficacia come analgesico (contro il dolore), antipiretico (contro la febbre) e anti-infiammatorio è ben documentata. Inoltre, a basse dosi, è utilizzato per le sue proprietà antiaggreganti piastriniche, nella prevenzione di eventi cardiovascolari come infarti e ictus.
La sua scoperta e la successiva sintesi su larga scala hanno rappresentato una pietra miliare nella storia della farmacologia, rendendo accessibile un trattamento efficace per una vasta gamma di disturbi.
Estrazione da Fonti Farmaceutiche
Un'alternativa alla sintesi chimica, discussa in contesti di forum online, è l'estrazione dell'acido acetilsalicilico da farmaci commerciali contenenti questo principio attivo, come ad esempio il Vivin C. Questo approccio, sebbene potenzialmente utile per ottenere il composto puro, presenta delle complessità legate alla separazione dell'acido acetilsalicilico dagli eccipienti presenti nelle formulazioni farmaceutiche. L'uso di solventi come l'alcool può portare all'estrazione di altre sostanze indesiderate, che richiedono ulteriori passaggi di purificazione.
Conclusione Provvisoria
La sintesi e la cristallizzazione dell'acido acetilsalicilico offrono un'eccellente opportunità per comprendere i principi fondamentali della chimica organica sintetica e delle tecniche di purificazione. La cura nella scelta dei reagenti, in particolare dell'anidride acetica, e l'attenzione meticolosa alla fase di cristallizzazione sono essenziali per ottenere un prodotto finale di alta purezza e qualità. L'acido salicilico, precursore dell'aspirina, vanta una storia ricca e applicazioni diversificate che vanno dalla farmacologia alla dermatologia e alla biologia vegetale.
tags: #cristallizzazione #di #acido #salicilico